 Katalysatoren
Katalysatoren
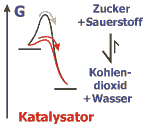
Katalysatoren reduzieren den Betrag der Aktivierungsenergie einer Reaktion und beschleunigen so die Einstellung des chemischen Gleichgewichts.
Im Beispiel ist die Verbrennung (Reaktion mit Sauerstoff) von Zucker zu Kohlendioxid und Wasser dargestellt. Obwohl wegen der freiwerdenden Energie das Gleichgewicht dieser Reaktion weit auf der Seite der Verbrennungsprodukte liegt, ist Zucker wegen der großen Aktivierungsenergie der Reaktion unter normalen Bedingungen sehr stabil. Die Verbrennung gelingt nur bei Zuführung einer größeren Energiemenge, die die Schwelle der Aktivierungsenergie überwinden hilft, oder bei Einsatz von Katalysatoren die diese Schwelle absenken.